Ley de Charles
Relación entre la temperatura y el volumen de un gas cuando la presión es constante
En 1787, Jack Charles estudió por primera vez la relación entre el volumen y la temperatura de una muestra de gas a presión constante y observó que cuando se aumentaba la temperatura el volumen del gas también aumentaba y que al enfriar el volumen disminuía.
Publicado por
Equipo Verde
en
16:02
0
comentarios
![]()
Ley de Boyle-Mariotte
http://www.youtube.com/watch?v=pGnNG4j1qog&feature=fvstLa Ley de Boyle-Mariotte (o Ley de Boyle), formulada por Robert Boyle y Edme Mariotte, es una de las leyes de los gases ideales que relaciona el volumen y la presión de una cierta cantidad de gas mantenida a temperatura constante. La ley dice que el volumen es inversamente proporcional a la presión: 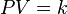
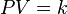
donde  es constante si la temperatura y la masa del gas permanecen constantes.
es constante si la temperatura y la masa del gas permanecen constantes.
 es constante si la temperatura y la masa del gas permanecen constantes.
es constante si la temperatura y la masa del gas permanecen constantes.Cuando aumenta la presión, el volumen disminuye, mientras que si la presión disminuye el volumen aumenta. El valor exacto de la constante k no es necesario conocerlo para poder hacer uso de la Ley; si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
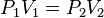
Además se obtiene despejada que:




Donde:
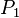 = Presión Inicial
= Presión Inicial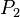 = Presión Final
= Presión Final = Volumen Inicial
= Volumen Inicial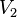 = Volumen Final
= Volumen Final
Esta Ley es una simplificación de la Ley de los gases ideales particularizada para procesos isotermos.
Junto con la ley de Charles y Gay-Lussac y la ley de Graham, la ley de Boyle forma las leyes de los gases, que describen la conducta de un gas ideal. Las tres leyes pueden ser generalizadas en la ecuación universal de los gases.
[editar] Experimento de Boyle
Para poder comprobar su teoría, Boyle hizo el experimento el cual ayudó a comprobar su teoría, es el siguiente: Introdujo un gas en un cilindro con un émbolo y comprobó las distintas presiones al bajar el émbolo. A continuación hay una tabla que muestra algunos de los resultados que obtuvo:
| × | P (atm) | V (L) | P · V |
|---|---|---|---|
| 0,5 | 60 | 30 | |
| 1,0 | 30 | 30 | |
| 1,5 | 20 | 30 | |
| 2,0 | 15 | 30 | |
| 2,5 | 12 | 30 | |
| 3,0 | 10 | 30 |
Si se observan los datos de la tabla se puede comprobar que al disminuir el volumen, la presión 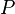 , aumenta y que al multiplicar
, aumenta y que al multiplicar 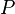 y
y  se obtiene
se obtiene  atm.L.
atm.L.
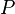 , aumenta y que al multiplicar
, aumenta y que al multiplicar 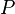 y
y  se obtiene
se obtiene  atm.L.
atm.L.
Publicado por
Equipo Verde
en
15:49
0
comentarios
![]()
Suscribirse a:
Entradas (Atom)


